การกลั่น (distillation)
การกลั่นเป็นการแยกสารละสายที่เป็นของเหลวออกจากของผสม โดยอาศัยหลักการระเหยกลายเป็นไปและควบแน่น โดนที่สารบริสุทธิ์แต่ละชนิดเปลี่ยนสถานะได้ที่อุณหภูมิจำเพาะ สารที่มีจุดเดือดต่ำจะเดือดเป็นไอออกมาก่อน เมื่อทำให้ไอของสารมีอุณหภูมิต่ำลงจะควบแน่นกลับมาเป็นของเหลวอีกครั้ง
1. การกลั่นแบบธรรมดาหรือการกลั่นอย่างง่าย (simple distillation)
2. การกลั่นลำดับส่วน (fractional distillation)
3. การกลั่นน้ำมันดิบ (refining)
4. การสกัดโดยการกลั่นด้วยไอน้ำ
1. การกลั่นแบบธรรมดาหรือการกลั่นอย่างง่าย (simple distillation)
เป็นวิธีการ ที่ใช้กลั่นแยกสารที่ระเหยง่ายซึ่งปนอยู่กับสารที่ระเหยยาก การกลั่นธรรมดานี้ จะใช้แยกสารออกเป็นสารบริสุทธิ์เพียงครั้งเดียวได้สารที่มีจุดเดือดต่างกัน ตั้งแต่ 80 องศาเซลเซียส ขึ้นไป
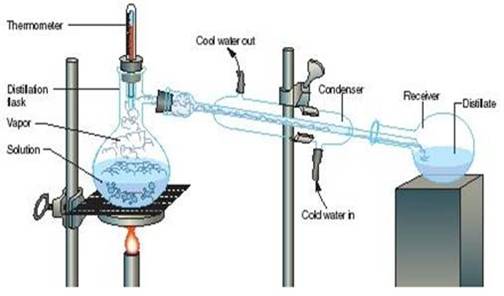
ภาพที่ 13 การกลั่นแบบธรรมชาติหรือการกลั่นแบบง่าย
ที่มา : http://www.lks.ac.th/student/kroo_su/chem11/sub07.html
เครื่องมือที่ใช้สำหรับการกลั่นอย่างง่าย ประกอบด้วย ฟลาสกลั่น เทอร์โมมิเตอร์ เครื่องควบแน่น และภาชนะรองรับสารที่กลั่นได้ การกลั่นอย่างง่ายมีเทคนิคการทำเป็นขั้น ๆ ดังนี้
1. เทของเหลวที่จะกลั่นลงในฟลาสกลั่น โดยใช้กรวยกรอง
2. เติมชิ้นกันเดือดพลุ่ง เพื่อให้การเดือดเป็นไปอย่างสม่ำเสมอและไม่รุนแรง
3. เสียบเทอร์โมมิเตอร์
4. เปิดน้ำให้ผ่านเข้าไปในคอนเดนเซอร์เพื่อให้คอนเดนเซอร์เย็น โดยให้น้ำเข้าทางที่ต่ำแล้วไหลออกทางที่สูง
5. ให้ความร้อนแก่พลาสกลั่นจนกระทั่งของเหลวเริ่มเดือด ให้ความร้อนไปเรื่อย ๆ จน กระทั่งอัตราการกลั่นคงที่ คือได้สารที่กลั่นประมาณ 2 - 3 หยด ต่อวินาที ให้สารที่กลั่นได้นี้ไหลลงในภาชนะรองรับ
6. การกลั่นต้องดำเนินต่อไปจนกระทั่งเหลือสารอยู่ในฟลาสกลั่นเพียงเล็กน้อยอย่ากลั่นให้แห้ง
การกลั่นสามารถนำมาใช้ทดสอบความบริสุทธิ์ของของเหลวได้ซึ่งของเหลว ที่บริสุทธิ์ จะมีลักษณะดังนี้
1. ส่วนประกอบของสารที่กลั่นได้ จะมีลักษณะเหมือนกับส่วนประกอบ ของของเหลว
2. ส่วนประกอบจะไม่มีการเปลี่ยนแปลง
3. อุณหภูมิของจุดเดือดในขณะกลั่นจะคงที่ตลอดเวลา
4. การกลั่นจะทำให้เราทราบจุดเดือดของของเหลวบริสุทธิ์ได้
การกลั่นนอกจากจะนำมาใช้ตรวจสอบ ความบริสุทธิ์ของของเหลวแล้วยังสามารถใช้กลั่นสารละลายได้อีกด้วย การกลั่นสารละลายเป็นกระบวนการแยกของแข็งที่ไม่ระเหยออกจากตัวทำละลายหรือ ของเหลวที่ระเหยง่าย โดยของแข็ง ที่ไม่ระเหยหรือตัวละลาย จะอยู่ในฟลาสกลั่น ส่วนของเหลวที่ระเหยง่ายจะถูกกลั่นออกมา เมื่อการกลั่นดำเนินไปจนกระทั่งอุณหภูมิของการกลั่นคงที่แสดงว่าสารที่เหลือนั้นเป็นสารบริสุทธิ์
อนึ่งในขณะกลั่นจะสังเกตเห็นว่าอุณหภูมิของสารละลายจะเพิ่มขึ้นเรื่อย ๆ เพราะสารละลายเข้มข้นขึ้น เนื่องจากตัวทำละลายระเหยออกไปและได้ของแข็งที่บริสุทธิ์ ในที่สุด
2. การกลั่นลำดับส่วน (fractional distillation)
การกลั่นลำดับส่วนเป็นวิธีการแยกของเหลวที่สามารถระเหยได้ตั้งแต่ 2 ชนิดขึ้นไป มีหลักการเช่นเดียวกันกับการกลั่นแบบธรรมดา คือเพื่อต้องการแยกองค์ประกอบในสารละลายให้ออกจากกัน แต่ก็จะมีส่วนที่แตกต่างจากการกลั่นแบบธรรมดา คือ การกลั่นแบบกลั่นลำดับส่วน เหมาะสำหรับใช้กลั่นของเหลวที่เป็นองค์ประกอบของ สารละลายที่จุดเดือดต่างกันน้อย ๆ ในขั้นตอนของกระบวนการกลั่นลำดับส่วน จะเป็นการนำไอของแต่ละส่วนไปควบแน่น แล้วนำไปกลั่นซ้ำและควบแน่นไอเรื่อย ๆ ซึ่งเทียบได้กับเป็นการกลั่นแบบธรรมดาหลาย ๆ ครั้งนั่นเอง ความแตกต่างของการกลั่นลำดับส่วนกับการกลั่นแบบธรรมดาจะอยู่ที่คอลัมน์ โดยคอลัมน์ของการกลั่นลำดับส่วนจะมีลักษณะเป็นชั้นซับซ้อน เป็นชั้น ๆ ในขณะที่คอลัมน์แบบธรรมดาจะเป็นคอลัมน์ธรรมดา ไม่มีความซับซ้อนของคอลัมน์
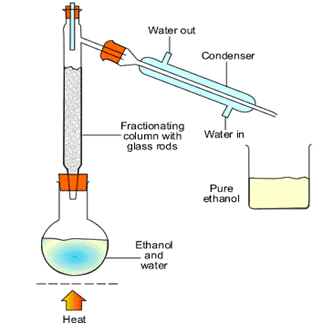
ภาพที่ 14 การกลั่นลำดับส่วน
ที่มา : http://www.lks.ac.th/student/kroo_su/chem11/sub07.html
ในการกลั่นแบบลำดับส่วน จะต้องมีการเพิ่มอุณหภูมิอย่างช้า ๆ ดังนั้น จำเป็นที่จะต้องมีอุปกรณ์ที่ให้ความร้อน (heater) และสามารถควบคุมอุณหภูมิได้ เพราะของผสมที่กลั่นแบบลำดับส่วนมักจะมีจุดเดือดที่ใกล้เคียงกัน ซึ่งตรงกันข้ามกับการกลั่นแบบธรรมดา ความร้อนที่ให้ไม่จำเป็นต้องควบคุมเหมือนการกลั่นลำดับส่วน แต่ก็ไม่ควรให้ ความร้อนที่สูงเกินไป เพราะความร้อนที่สูงเกินไป อาจจะไปทำลายสารที่เราต้องการกลั่นเพราะฉะนั้นประสิทธิภาพในการกลั่นลำดับส่วนจึงดีกว่าการกลั่นแบบธรรมดา
3. การกลั่นน้ำมันดิบ (refining)
เนื่องจากน้ำมันดิบ ประกอบด้วยสารประกอบไฮโดรคาร์บอนหลายพันชนิด ดังนั้นจึงไม่สามารถแยกสารที่มีอยู่ออกเป็น สารเดี่ยว ๆ ได้ อีกทั้งสารเหลวนี้มีจุดเดือดใกล้ เคียงกันมากวิธีการแยกองค์ประกอบน้ำมันดิบจะทำได้โดยการกลั่นลำดับส่วนและเก็บสาร ตามช่วงอุณหภูมิ ซึ่งก่อนที่จะกลั่นจะต้องนำน้ำมันดิบมาแยกเอาน้ำ และสารประกอบกํามะถัน ออกซิเจน ไนโตรเจนและโลหะหนักอื่น ๆ ออกไปก่อนที่จะนำไปเผาที่อุณหภูมิ 320 - 385 C0 ผลิตภัณฑ์ที่ได้จากการกลั่น ได้แก่
- ก๊าซ (C1 - C4) ซึ่งเป็นของผสมระหว่างก๊าซมีเทน อีเทน โพรเพนและบิวเทน เป็นต้น ประโยชน์ : มีเทนใช้เป็นเชื้อเพลิงผลิตกระแสไฟฟ้า อีเทน โพรเพนและบิวเทน ใช้ในอุตสาหกรรม
- ปิโตรเคมี และโพรเพน และบิวเทนใช้ทําก๊าซหุงต้ม (LPG)
- แนฟทาเบา (C5 - C7) ประโยชน์ : ใช้ทําตัวทําละลาย - แนฟทาหนัก (C6 - C12) หรือ เรียกว่าน้ำ
- มันเบนซินประโยชน์ : ใช้ทําเชื้อเพลิงรถยนต์
- น้ำมันก๊าด (C10 - C14) ประโยชน ์ : ใช้ทําเชื้อเพลิงสําหรับตะเกียง และเครื่องยนต์
- น้ำมันดีเซล (C14 - C19) ประโยชน์ : ใช้ทําเชื้อเพลิงเครื่องยนต์ดีเซล ได้แก่ รถบรรทุก , เรือ
- น้ำมันหล่อลื่น (C19 - C35) ประโยชน์: ใช้ทําน้ำมันหล่อลื่นเครื่องยนต์เครื่องจักรกล - ไขน้ำมันเตาและยางมะตอย (C > C35)
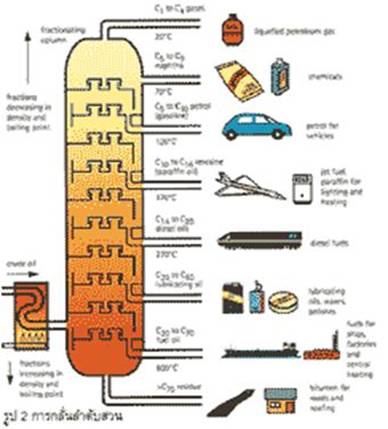
ภาพที่ 15 การกลั่นน้ำมันดิบ
ที่มา : http://www.lks.ac.th/student/kroo_su/chem11/sub07.html
4. การสกัดโดยการกลั่นด้วยไอน้ำ
เป็นวิธีการสกัดสารออก จากของผสมโดยใช้ไอน้ำเป็นตัวทำละลาย วิธีนี้ใช้สำหรับแยกสารที่ระเหยง่าย ไม่ละลายน้ำ และไม่ทำปฏิกิริยากับน้ำออกจากสาร ที่ระเหยยาก การสกัดโดยการกลั่นด้วยไอน้ำ นอกจากใช้สกัดสารระเหยง่าย ออกจาก สารระเหยยากแล้วยังสามารถใช้แยกสารที่มีจุดเดือดสูง และสลายตัวที่จุดเดือด ของมันได้อีก เพราะการกลั่นโดยวิธีนี้ความดันจะเป็นความดันไอน้ำบวกความดันไอน้ำของของเหลวที่ต้องการแยก จึงทำให้ความดันไอน้ำเท่ากับความดันของบรรยากาศก่อนที่อุณหภูมิจะถึงจุดเดือดของ ของเหลวที่ต้องการแยกของผสมจึงกลั่นออกมา ที่อุณหภูมิต่ำกว่าจุดเดือดของของเหลวที่ต้องการแยก เช่น สาร A มีจุดเดือด 150 C0 เมื่อสกัดโดยการกลั่นด้วยไอน้ำจะได้สาร A กลายเป็นไอออกมา
ณ อุณหภูมิ 95 C0 ที่ความดัน 760 มิลลิเมตร ของปรอท อธิบายได้ว่า ที่ 95 C0 ถ้าความดันไอน้ำของสาร A เท่ากับ 120 มิลลิเมตร ของปรอท และไอน้ำเท่ากับ 640 มิลลิเมตรของปรอท เมื่อความดันไอน้ำของสาร A รวมกับไอน้ำจะเท่ากับ 760 มิลลิเมตรของปรอท หรือเท่ากับความดันบรรยากาศ จึงทำให้สาร A และน้ำกลายเป็นไอออกมาได้ที่อุณหภูมิต่ำกว่าจุดเดือด ของสาร A ตัวอย่างการแยกสารโดยการกลั่นด้วยไอน้ำ
การแยกน้ำมันหอมระเหยออกจาก ส่วนต่าง ๆ ของพืช เช่น การแยกน้ำมัน ยูคาลิปตัสออกจากใบยูคาลิปตัสการแยกน้ำมันมะกรูด ออกจากผิวมะกรูดการแยกน้ำมันอบเชยจากเปลือกต้นอบเชย เป็นต้น ในการกลั่นไอน้ำจะไปทำให้น้ำมันหอมระเหยกลายเป็นไอแยกออกมาพร้อมกับไอน้ำ เมื่อทำให้ไอของของผสมควบแน่น โดยผ่านเครื่องควบแน่นก็จะได้น้ำและน้ำมันหอมระเหยปนกัน แต่แยกชั้นกันอยู่ ทำให้สามารถแยกเอาน้ำมันหอมระเหยออกจากน้ำได้ง่าย
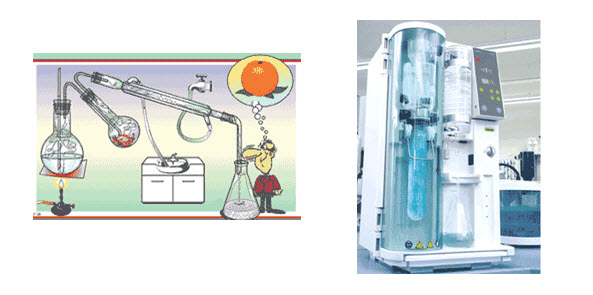
ภาพที่ 16 การกลั่นด้วยไอน้ำ
ที่มา : http://www.lks.ac.th/student/kroo_su/chem11/sub07.html
|